Questions
- What is the pH?
- ==pH is a measure of the acidity or basicity of a solution.
It is defined as the negative logarithm (base 10) of the concentration of hydrogen ions (H+) in a solution==.
==A pH of 7 is considered neutral, meaning that the concentration of H+ ions is equal to the concentration of hydroxide (OH-) ions==.
Solutions with a pH lower than 7 are acidic, indicating a higher concentration of H+ ions, while solutions with a pH greater than 7 are basic (also called alkaline), indicating a higher concentration of OH- ions.
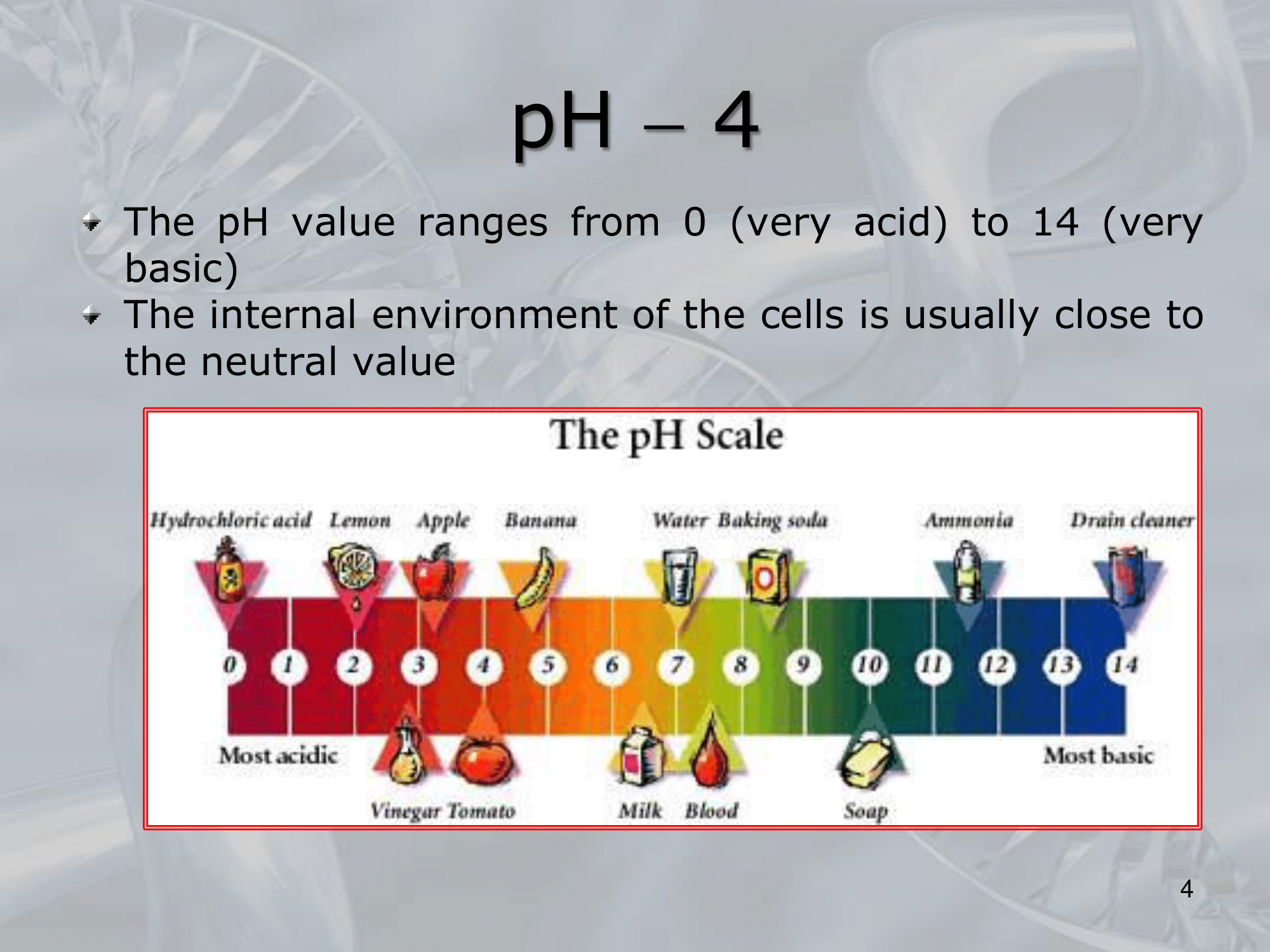
The pH scale ranges from 0 to 14, with lower numbers indicating more acidity and higher numbers indicating more basicity.
Changes in pH can have significant effects on biological systems, as many enzymes and other biomolecules are sensitive to pH and may only function properly within a narrow pH range.
- ==pH is a measure of the acidity or basicity of a solution.
—————————————————————
IMPORTANTE
IMPORTANTE Mole ed il Numero di Avogadro:

IMPORTANTE pH:


Più molecole di ci sono più una soluzione è acida (pH = 0 ⇒ l’intera mole è costituita da ) Più molecole di ci sono più una soluzione è basica (pH = 14 ⇒ la concentrazione di in una singola mole è pari a: ) #IMPORTANTE La formula del pH è: dove è la concentrazione di **ioni positivi di idrogeno
—————————————————————
Slides with Notes

IMPORTANTE Mole ed il Numero di Avogadro:


IMPORTANTE pH:


Più molecole di ci sono più una soluzione è acida (pH = 0 ⇒ l’intera mole è costituita da ) Più molecole di ci sono più una soluzione è basica (pH = 14 ⇒ la concentrazione di in una singola mole è pari a: ) #IMPORTANTE La formula del pH è: dove è la concentrazione di ioni positivi di idrogeno